会员风采 | IND获批!茵冠生物“人脐带间充质干细胞注射液”正式获批临床试验
时间:2023-03-22 10:03
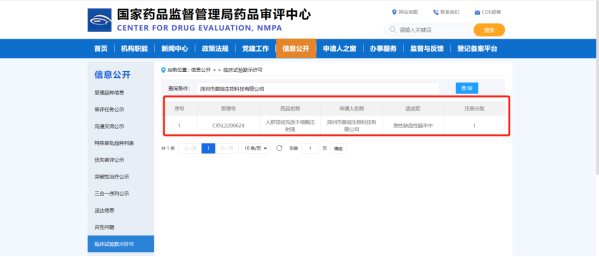
▲国家药监局官网:茵冠生物“人脐带间充质干细胞注射液”获临床试验默示许可
CDE,即国家药品监督管理局药品审评中心,是国家食品药品监督管理局药品注册技术审评机构,按照国家食品药品监督管理局颁布的药品注册管理有关规章,负责组织对药品注册申请进行技术审评,组织开展相关的综合评审工作。
IND,即新药临床试验,是药物研发企业以注册目的,在药品正式上市前,向CDE提供足够信息来证明药品在人体进行试验是安全的,以及证明针对研究目的的临床方案设计是合理的而开展的人体临床试验。
脑卒中是我国成年人致死和致残的首位原因。国家卫健委2021年最新发布的统计数据显示,我国脑卒中患病总人数超过2800万,每5位死亡者中就至少有1人死于脑卒中。
急性缺血性脑卒中(AIS)早期诊断和治疗至关重要,目前常用的溶栓治疗不能逆转神经细胞数量日益减少所导致的功能障碍;血管重建手术存在出血、感染等并发症风险。
而干细胞成药的关键在于“质量”的稳定、可控与“治疗”的安全、有效。茵冠生物遵循干细胞药品研发、生产、质控等相关国际及国内标准建设了B+A级大规模生产制备及质控平台,并建立起一整套严苛的高于国际标准的质量管理体系,通过了ISO9001质量体系认证,以高标准的硬件设施与成熟的工艺质控最大限度地保证每批次细胞制品质量的均一性和稳定性,生产的核心产品“人脐带间充质干细胞”通过国内三甲医院唯一认可、国家权威第三方质量检测机构——中国食品药品检定研究院的质量复核检验。
以上信息来源:茵冠生物
副会长单位简介
——深圳市茵冠生物科技有限公司
深圳市茵冠生物科技有限公司是一家致力于细胞治疗领域,聚焦于干细胞创新药物及疗法,集研究、开发、转化及应用的高科技企业,获得美瑞健康国际(HK02327)、汉商集团(SH.600774)、知名投资机构东方富海GP-深圳市政府引导基金子基金战略投资。
茵冠生物拥有干细胞技术、免疫细胞技术和基因编辑技术三大平台,建设数千平符合国际cGMP标准的“B+A”级生产研发基地,该基地是深圳市发改委备案的“华南综合细胞库”、“华南区域细胞制备中心”。
在线评论
| 匿名 |
-
暂无记录
